20世纪70年代美国学者Fisher首先提出:乳腺癌一开始就是一种全身性疾病,原发灶和区域淋巴结的处理方式不会影响患者的生存率。全球多项极具代表性的前瞻性随机对照试验,对乳腺癌保乳手术与乳房切除手术的疗效进行了比较,均证实了保乳手术的可行性,同时也肯定了术后放疗的必要性。1995年,早期乳腺癌试验协作组(EBCTCG)报道了保乳手术加放疗与乳房切除手术两组疗效对比的meta分析结果,10年死亡率均为22.9%,10年局部复发率分别为5.9%和6.2%,两组比较无统计学差异(表27-1、表27-2)。
表27-1 保乳手术+放疗与乳房切除手术临床研究分析
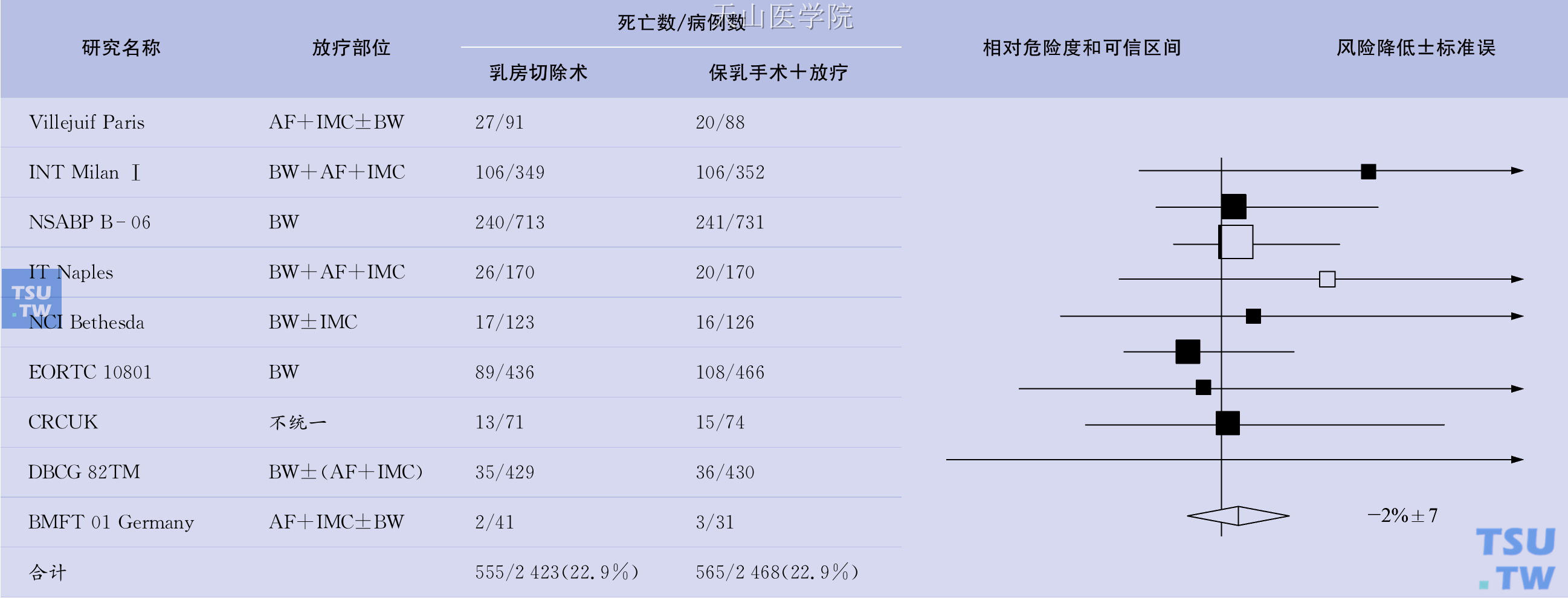
注:方形图标代表保乳手术+放疗组与乳房切除手术组相比10年死亡率的相对危险度,垂直线代表相对危险度为1,水平线代表99%可信区间。AF:腋窝或锁骨上窝;IMC:内乳区淋巴链;BW:乳房或胸壁。Villejuif Paris:法国巴黎古斯塔夫卢西研究所。INT Millan I:意大利米兰肿瘤治疗研究所。NSABP B-06:国家乳腺和肠道外科辅助治疗计划(美国匹兹堡)。IT Naples:意大利那不勒斯肿瘤研究所。NCI Bethesda:美国国立癌症研究所(马里兰州贝塞斯达)。EORTC 10801:欧洲癌症治疗和研究组织(比利时布鲁塞尔)。CRCUK:癌症研究项目(英国伦敦)。Danish BCG 82TM:丹麦乳腺癌协作组(哥本哈根)。BMFT 01 Germany:德国联邦研究和技术部(弗莱堡)。
表27-2 保乳手术+放疗与乳房切除手术的10年局部复发率
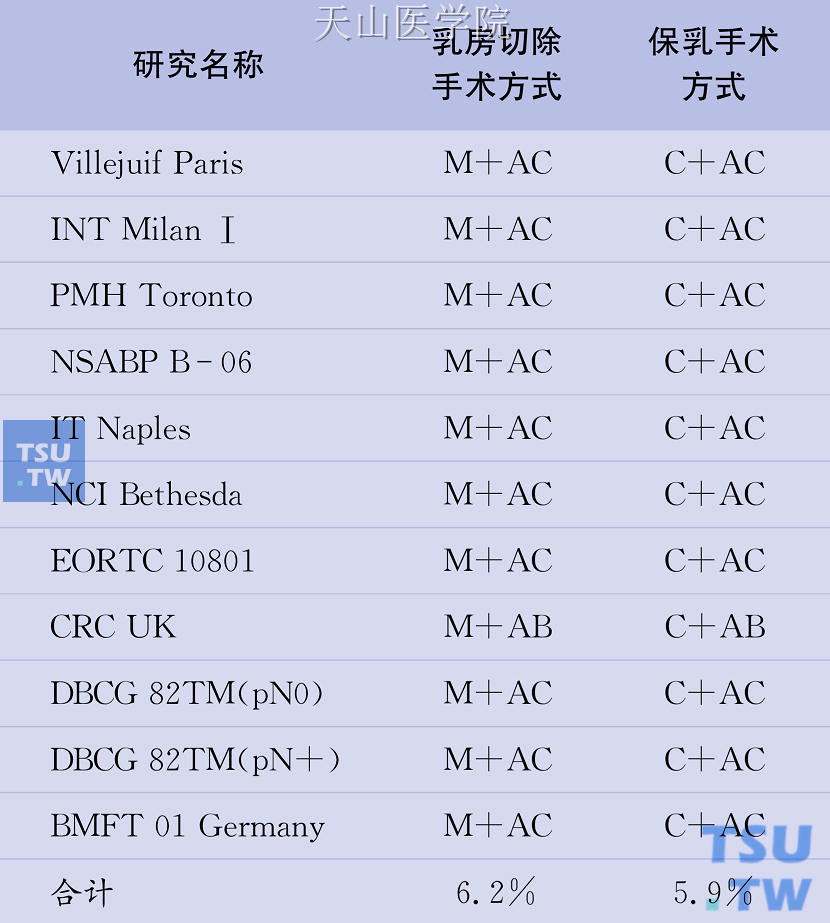
注:M:乳房切除术;AC:腋窝淋巴结清扫;AB:腋窝淋巴结活检;C:保乳手术。
20世纪80年代全球各大癌症中心达成共识,保乳手术加放疗可以取得与乳房切除手术同样的疗效。Fisher称保乳手术是对Halsted学派的挑战,是乳腺癌外科治疗中的一次革命。保乳手术成为治疗早期乳腺癌优先考虑的手术术式。美国外科医师协会、放射治疗医师协会、病理医师协会以及肿瘤外科协会就保乳治疗提出了规范化实施意见。国际上较权威的NIH、NCCN、St.Gallen对乳腺癌的保乳治疗提出了指导性建议。日本乳腺癌学会于1999年公布了保乳疗法指南,对其定义、适应证、治疗方法、病理诊断、评价及放疗技术进行了详尽的阐述。保乳手术不仅提高患者生存率、降低复发率,还要兼顾生活质量和形体效果。目前,乳腺癌保乳手术在美国占全部乳腺癌手术的50%以上,日本超过40%。
中国乳腺癌保乳手术概况
中国乳腺癌保乳手术始于20世纪50年代。中国医学科学院肿瘤医院从1958年就开始为个别患者实施保乳手术加术后放疗。当时并不是出于临床研究目的,而是针对临床上年迈体弱或合并其他慢性疾病不能耐受Halsted手术及其麻醉而采取的治疗选择。中国自20世纪80年代中期,少数医院开始为部分I、Ⅱ期乳腺癌患者实施保乳手术加根治性放疗;90年代以后,我国一些医院对保乳手术的适应证、切口设计、腋窝淋巴结清扫范围以及术后放疗进行了研究,形成了初步共识。下面就文献报道举例说明:中国医学科学院肿瘤医院,1985年1月至2001年12月共实施保乳手术206例,3年、5年、10年生存率分别为99%、94%、80%,局部复发率分别为5.4%、7.0%、7.7%;保乳治疗结束后有167例患者回本院复查进行美容效果评估,优、良者总和为139例,占83.2%。天津医科大学附属肿瘤医院,1989年7月至2003年2月共完成保乳手术185例,中位年龄41岁(23~80岁),全组随访4~168个月。随访满5年患者的总生存率98.8%(79/80),无瘤生存率96.3%(77/80),局部复发率1.3%(1/80),远处转移率3.8%(3/80);随访满10年患者的总生存率86.4%(19/22),无瘤生存率81.8%(18/22),局部复发率13.6%(3/22),远处转移率18.2%(4/22)。复旦大学附属肿瘤医院,1995年10月至2004年7月完成保乳手术234例,患者中位年龄43.5岁(25~85岁),中位随访期22个月(3~100个月),3年总生存率96.7%。复旦大学附属中山医院,1995年1月至2004年12月共收治女性乳腺癌2 548例,选择0~ⅡA期、非乳晕区单发肿瘤247例施行保乳手术,占同期全部乳腺癌手术的9.7%(247/2 548)。平均随访69个月,随访率74.1%(183/247),局部复发率1.6%(3/183),5年无病生存率95.6%(175/183);美容效果评估优者144例,良者89例,差者14例,总满意率为93.6%。
中国医学科学院肿瘤医院联合其他9家三甲医院共同完成的国家“十五”科技攻关课题——早期乳腺癌规范化保乳综合治疗的多中心研究(2001年11月至2004年11月),这是我国首项乳腺癌保乳综合治疗的前瞻性、多中心研究。本研究非随机化,在适合保乳的病例中根据患者的选择分为保乳治疗组和切除乳房治疗组。3年共完成保乳手术872例,乳房切除手术3 589例。若加上不符合保乳手术适应证的病例,同期所有经手术治疗的乳腺癌病例为9 726例。保乳手术占符合保乳条件病例的19.5%,占全部乳腺癌手术病例的9.0%。随访结果:保乳治疗组复发9例(1.0%),远处转移11例(1.3%),死亡1例(0.1%);切除乳房治疗组复发18例(0.5%),远处转移49例(1.4%),死亡4例(0.1%),两组间无统计学差异(P>0.05)。保乳术后美容效果评估:优、良者术后6个月为89.1%,术后1年为91.1%,术后2年为86.6%。据中国女性原发性乳腺癌10年(1999~2008年)抽样回顾性调查数据显示(图27-1),保乳手术比例不高,呈上升趋势,1999年仅占乳腺癌手术的1.29%,到2008年也仅占11.57%,但10年上升了10.28个百分点(X2=102.835,P<0.001)。
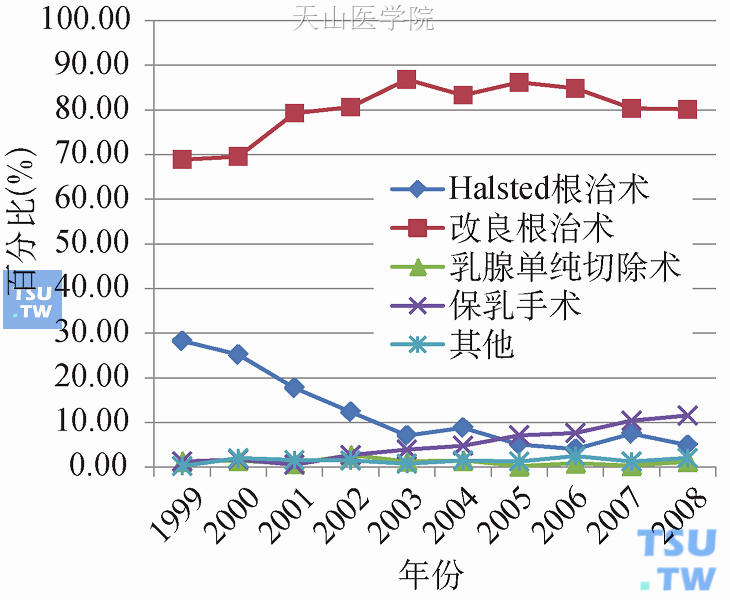
图27-1 1999~2008年中国乳腺癌手术治疗方式的变化趋势
中国乳腺癌保乳手术比例明显低于欧美国家,究其原因与患者就诊时的病期、治疗观念、医疗技术、放疗设备以及患者的经济状况等诸多因素有关。近年中国少数三甲医院完成保乳手术的例数约占全部乳腺癌手术的30%。中国开展的保乳手术在适应证的选择、保乳手术切缘的检测、术后美容效果评估标准等方面均与欧美国家存在差异,整体而言规范化不足,随意性较大。随着我国乳腺癌筛查项目的规范化,保乳治疗理念逐步被社会所接受,放疗设备逐渐普及,以及新辅助化疗和肿瘤整形外科(oncoplastic surgery)技术拓展了保乳手术的可行性空间,保乳治疗也必将成为中国早期乳腺癌的主要治疗模式。
保乳手术的适应证和禁忌证
卫生部组织制定的《乳腺癌诊疗规范(2011年版)》参考了《NCCN乳腺癌临床实践指南》和我国保乳手术的实践经验,提出了乳腺癌保乳手术的适应证和禁忌证。
(1)适应证:保乳手术适用于患者有保乳意愿;乳腺肿瘤可以完整切除,达到阴性切缘,并可获得良好的美容效果;年轻不作为保乳手术的禁忌,≤35岁的患者有相对高的复发和再发乳腺癌的风险,在选择保乳时,应向患者充分交待可能存在的风险。
(2)禁忌证:保乳手术的绝对禁忌证包括既往接受过乳腺或胸壁放疗;妊娠期需放疗;病变广泛无法完整切除;最终切缘阳性。相对禁忌证包括肿瘤直径>5cm和累及皮肤的活动性结缔组织病,尤其是硬皮病和系统性红斑狼疮。
保乳手术有关的问题及注意事项
患者的知情同意
中国乳腺癌科普知识的宣传不够,非医务界人士对乳腺癌保乳治疗缺乏了解,特别是一些患者自认为诊断为乳腺癌就必须切除乳房,保留乳房治疗会不彻底,容易复发,对保乳手术没有信心和需求。Katz等评价了患者在乳腺癌保乳治疗决策中的作用。在一个以白种人女性乳腺癌为基础且无保乳治疗禁忌证的人群中,当患者以外科医师为首要决策时,决定行乳房切除手术仅为5.3%,当医患双方共同决策时为16.8%,当患者自己做决策时则升至27%(P<0.000 1)。由于多数患者不了解循证医学的最新结果,不能及时了解乳腺癌临床研究的最新进展,选择手术方式时存在一定的局限性。患者表示在决策过程中癌症复发是她们考虑的首要因素,因此我国《乳腺癌诊疗规范(2011年版)》中保乳手术适应证首先提到的就是患者有保乳意愿。
年龄
中国开展保乳手术在年龄上与欧美国家出现反差,基于年轻患者对保留乳房需求迫切,而老年患者往往要求不高,结果经保乳治疗患者与欧美国家相比以年轻患者居多,包括≤35岁者,而老年患者偏少。年轻患者保乳术后复发风险有多高?是否适合保乳?国内没有循证医学证据。
欧美国家对保乳手术按年龄分组进行过对照研究,保乳手术≤35岁组与>35岁组局部复发率的随访结果:美国宾夕法尼亚大学(UPenn)两组分别为24%和14%~15%;欧洲癌症治疗研究组织和丹麦乳腺癌协作组(EORTC和DBCG)两组分别为35%和9%;荷兰Leiden大学两组分别为28%和9%。可见保乳术后局部复发率≤35岁组大约是>35岁组的2~3倍。作为美国21家顶尖肿瘤中心组成的学术组织——NCCN制定的《NCCN乳腺癌临床实践指南》(2011年),曾将≤35岁浸润性乳腺癌列为保乳手术的相对禁忌证,并提出在选择保乳手术时,医师应向患者充分交代可能存在的风险。荷兰癌症研究所Rutgers在2009年3月瑞士召开的第11届St. Gallen国际乳腺癌大会上报告:保乳治疗15年后随访(绝大多数为切缘阴性),<41岁的乳腺癌患者同侧乳腺癌复发率为23%。辅助的系统治疗(内分泌治疗、化疗或两者联合应用)可适当降低这种高复发率(影响因子0.52),瘤床补充放射16Gy也能起到同样的作用。然而,尽管保乳术后采用充分的辅助治疗,10年后局部复发率仍达到15%左右,这个数据是>50岁保乳患者的2倍。EBCTCG研究观察得出“4对1”规律,即肿瘤长期局部生长导致远处转移的发生为每4例出现局部复发的乳腺癌将会增加1例死于远处转移的病例,故提出在所有复发风险的因素中,年龄是局部复发风险增加2倍的相关因素。
我国不是乳腺癌高发国家,发病年龄与欧美国家有所区别。<20岁乳腺癌罕见,<30岁少见,从30岁开始随年龄增加乳腺癌发病率逐渐上升,40~60岁是我国乳腺癌的高发年龄段。上海市疾病预防控制中心统计数据显示:绝经前乳腺癌占56%,而绝经后乳腺癌占44%。中国医学科学院肿瘤医院10年统计,原发性乳腺癌手术患者7 490例,其中≥65岁老年人乳腺癌1 231例,占16.4%。在美国,年龄越大患乳腺癌的风险越大,统计数据显示85岁为乳腺癌发病高峰,<36岁的乳腺癌非常少见,不到乳腺癌总数的5%。欧美国家新诊断的乳腺癌中≥65岁患者约占一半。
我们既要重视欧美国家循证医学的证据,又要结合中国妇女乳腺癌发病的特点,对年轻乳腺癌患者行保乳治疗应持慎重态度。年轻患者要求保乳应结合患者的发病情况、肿瘤分期、已知的有关生物学指标,确定能否保乳。卫生部组织制定的《乳腺癌诊疗规范(2011年版)》指出:年轻不作为保乳手术的禁忌,但≤35岁的患者有相对高的复发和再发乳腺癌的风险。在选择保乳时,应向患者充分交代可能存在的风险。对行保乳手术复发风险较大的年轻患者,可向其推荐保留皮肤的全乳切除加即刻乳房重建手术,以期在保证疗效的前提下,提高生活质量。对老年人乳腺癌,结合其特有的生物学行为,恶性程度相对较低,保乳手术创伤小,围术期并发症少,只要身体状况良好,无手术禁忌,有保乳需求,应积极开展保乳治疗。
肿瘤大小
在欧美国家肿瘤大小仅仅是能否保乳的一个方面,同时还要考虑肿瘤大小与乳房大小的比例。《NCCN乳腺癌临床实践指南》依据2B类共识提出,肿瘤>5cm为保乳手术的相对禁忌证,若经新辅助化疗后肿瘤缩小仍可行保乳手术。肿瘤虽较大,但患者乳房大,肿瘤广泛切除后仍可获得较理想的保乳效果,也可保乳。
中国妇女乳房发育总体较西方妇女小,故大多数医院保乳手术均选择肿瘤≤3cm;对3~5cm肿瘤可先行新辅助化疗,肿瘤缩小后再行保乳手术;少数医院保乳手术选择肿瘤在4cm以内。我国《乳腺癌诊疗规范(2011年版)》也将肿瘤直径>5cm作为保乳手术的相对禁忌证。就肿瘤大小确定患者是否适合行保乳手术,应结合就诊医院的技术水平、设备条件及患者的经济状况,统筹决定。强调重视肿瘤大小与乳房大小的比例,若乳房较小,选择保乳病例应区别于欧美国家;若为大乳房,选择保乳时,肿瘤大小可适当放宽。
肿瘤部位
乳腺癌可以发生在乳腺的周围象限,也可以发生在乳腺的中央区。乳腺癌的好发部位是外上象限,周围象限依次递减为内上象限、外下象限、内下象限。中央区乳腺癌文献报道占5%~20%。周围象限乳腺癌若符合保乳手术适应证可采用保乳治疗;中央区乳腺癌行保乳手术需切除乳头乳晕复合体,现有的研究数据尚不足以支持保留乳头乳晕复合体的手术。澳大利亚慈善姐妹医院Huemer等治疗中央区乳腺癌采用保乳手术,介绍了几种行肿瘤局部切除即刻乳房重建的外科技术,如肿瘤切除后直接关闭切口,应用倒T形切口,采用Benelli环乳晕切口,或改良的Grisotti瓣(B形切口)及应用下蒂的乳房缩小成形术等。全组无复发病例,并且取得了令人满意的美容效果。
肿瘤多中心及多灶性分布
乳腺不同象限同时出现癌灶,为乳腺癌的多中心分布;同一象限主癌灶周围出现癌灶,为乳腺癌的多灶性。欧美国家强调保乳手术前(通常指术前3个月内),应在高质量的乳腺X线机下进行乳腺X线摄片,进一步确定病灶的位置、大小,排除多中心病灶,并了解对侧乳腺的情况。也可以采用MRI来排除乳腺癌的多中心多灶问题。若乳腺X线片显示乳腺内弥漫性微小钙化灶并伴有恶性征象,需经组织病理学证实。
乳腺癌呈现多中心或多灶分布时行保乳手术需同时满足以下3个条件:①手术仅限一个切口(一个标本);②切缘阴性;③能获得良好的美容效果。《NCCN乳腺癌临床实践指南》(2011年)明确指出,病变广泛者,不可能通过单一切口的局部切除达到切缘阴性,且不致影响美观,则为保乳手术的绝对禁忌证。国内多数大医院也采用同样做法。但有些医院不具备乳腺X线机或MRI机,此项术前检查未列入保乳手术常规,在没有排除多中心病灶存在的前提下难以保证切缘阴性。
保乳手术切口设计及腋窝淋巴结清扫范围
美国国家乳腺和肠道外科辅助治疗计划(National Surgical Adjuvant Breast and Bowel Project,NSABP)推荐,乳腺癌保乳手术肿瘤切除的切口设计是以乳头为中心将乳腺分为上、下两部分,肿瘤位于乳头上方者行平行于乳晕的弧形切口,肿瘤位于乳头两侧者行沿乳头的水平切口,肿瘤位于乳头下方者行以乳头为中心的放射状切口(图27-2)。腋窝解剖的切口设计为平行于腋褶线的下方2cm的弧形切口,前端不超过胸大肌外侧缘,后端不超过背阔肌前缘,长5~6cm(图27-3)。有的医院对位于外上象限的肿瘤采用斜向腋窝的单一切口,既可切除肿瘤,又可清扫腋窝淋巴结,但术后乳房形体效果不如两切口为佳。
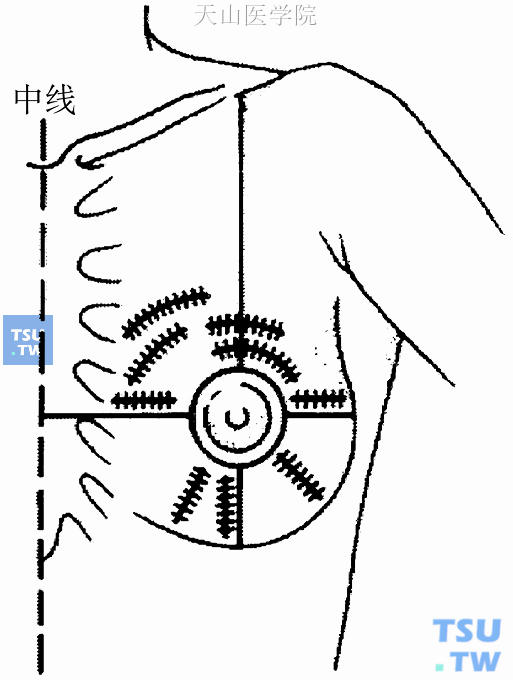
图27-2 NSABP推荐保乳手术肿瘤切除的切口设计
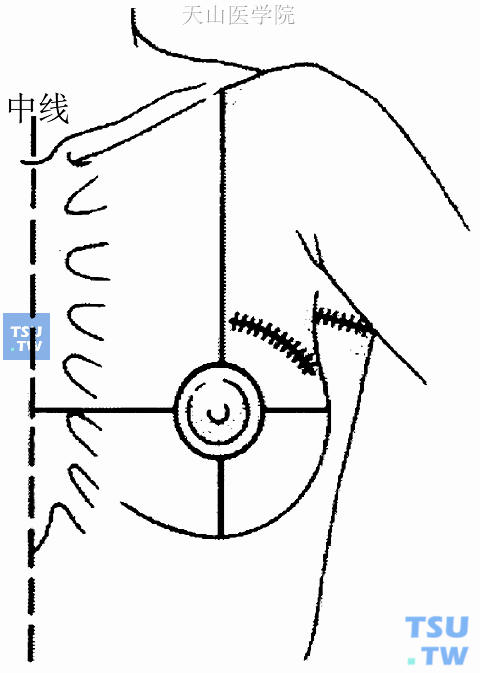
图27-3 NSABP推荐保乳手术中腋窝淋巴结清扫与乳腺肿瘤切除以两切口为宜
腋窝淋巴结手术是浸润性乳腺癌标准手术的一部分,其主要目的是了解腋窝淋巴结的状况,确定分期,选择最佳治疗方案。腋窝淋巴结的清扫范围应包括I水平(背阔肌前缘至胸小肌外侧缘)、Ⅱ水平(胸小肌外侧缘至胸小肌内侧缘)的所有淋巴结(图27-4)。保乳手术清扫腋窝淋巴结由于切口小,解剖范围广,手术操作要精细。清扫腋窝淋巴结的数目平均要求在10个以上,以保证能真实地反映腋窝淋巴结的状况。病理科医师应在切除的标本中尽量寻找淋巴结,逐个进行组织学检查。对有条件开展前哨淋巴结活检(sentinel lymph node biopsy,SLNB)的医院推荐对临床腋窝淋巴结无明确转移的患者开展前哨淋巴结活检。通过切除前哨淋巴结,再经病理组织学、细胞学和分子生物学诊断来了解腋窝淋巴结的状况,减少因腋窝淋巴结清扫导致的上肢淋巴水肿等并发症的发生。
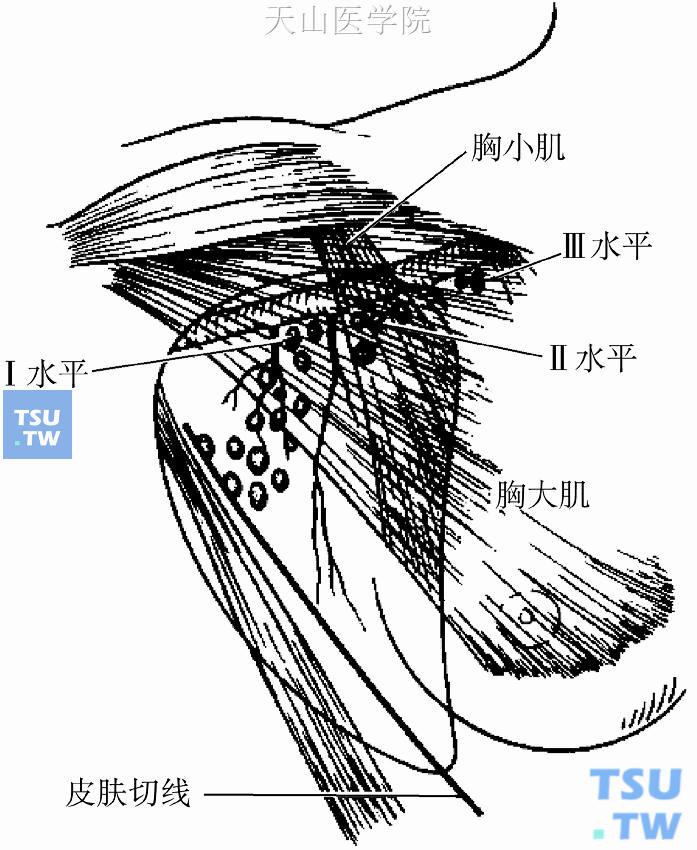
图27-4 腋窝淋巴结的清扫范围(I、Ⅱ水平)
保乳手术切除乳腺皮肤的问题
保乳手术适用于早期乳腺癌不包括TNM分期中的T4患者,即肿瘤已侵犯胸壁或皮肤,所以不需要切除肿瘤表面的过多皮肤。如穿刺或开放手术活检后行保乳手术,需切除穿刺针道或外科手术活检瘢痕,并酌情行切缘检测。
保乳手术的安全切缘
保乳手术原发灶的切除大体有3种术式:①乳房肿瘤切除术(lumpectomy),由Fisher倡导,需切除肿瘤周围1cm的乳腺组织,该术式在美国广泛应用;②肿瘤广泛切除术(wide excision),需切除肿瘤周围2~3cm的乳腺组织;③乳房象限切除术(quadran-tectomy),需切除肿瘤所在象限的全部乳腺组织、胸肌筋膜及部分皮肤,欧洲一些国家采用该术式。原发灶的切除要立足于肿瘤的完整切除,同时也要考虑局部形体效果。我国妇女乳房较小,保乳手术大多采用乳房肿瘤切除术或肿瘤广泛切除术。欧美国家非常重视保乳手术的切缘检测,主要依据切缘的组织学诊断。手术标本常规进行上、下、内、外、基底切缘的定位标记并染色,以利于病理科医师检测和报告。
保乳手术对切缘的要求是病理检查切缘阴性,希望切缘距瘤缘之间有一条没有肿瘤组织的条形带。但究竟多宽为安全,到目前为止尚缺乏循证医学证据。乳腺癌保乳与切除乳房治疗的6项前瞻性随机对照试验中,只有NSABPB - 06将切缘组织学阴性定义为肿瘤没有接触到染色区(染色的切缘无肿瘤),至于无瘤切除范围未作具体说明。2005年意大利米兰保乳共识会议上大多数放射肿瘤学专家认为,浸润性导管癌安全切缘至少1~2mm;若切缘冷冻切片阳性或广泛的导管内癌成分(extensive intraductal component, EIC)应再扩切;若多次阳性应放弃保乳手术。广泛的导管内癌成分是指在浸润性导管癌中,肿瘤体积的25%以上是导管原位癌(DCIS),且DCIS的分布范围超过了浸润性癌,已伸展至周围正常的乳腺组织中。乳腺导管内癌成分的诊断需要依靠石蜡切片检查,若镜下仅发现局灶性阳性切缘,不伴有EIC,选择保乳手术也是合理的,但术后必须考虑对瘤床部位实施高剂量的照射。若伴有EIC,或不能保证瘤床推量照射,只能再次手术,切除乳房,可考虑I期乳房重建。美国费城Fox Chase癌症中心O'Sullivan等对在保乳手术中为确保肿瘤切缘阴性而多次切缘送检的情况进行了研究,25年间保乳手术2 770例,分为3组,A组137例接受了超过2次的切缘再送检,B组1 514例接受了1次的切缘再送检,C组1 119例未接受切缘的再送检。A、B、C组的5年、10年局部复发率分别为5.5%、1.9%、2.5%和10%、5.7%、5.6%。多因素分析显示,在保证切缘阴性的情况下,术中多次肿瘤切缘送检并未影响保乳手术的局部复发率。
国外多数医院的冷冻检查室就设在手术室内,便于外科医师和病理科医师相互沟通。手术医师可以请病理科医师对送检标本的某一部位进行冷冻切片检查,病理科医师也可以建议手术医师对标本的某处邻近部位再次取材送检。
保乳手术的放疗
保乳术后放疗已成为规范化保乳治疗的重要组成部分。早期乳腺癌临床协作组(EBCTCG)随机对照的meta分析结果:保乳手术加放疗10年局部复发率为7.2%,而保乳手术不加放疗10年复发率高达22%(表27-3)。
表27-3 保乳术后放疗与不放疗的10年局部复发率
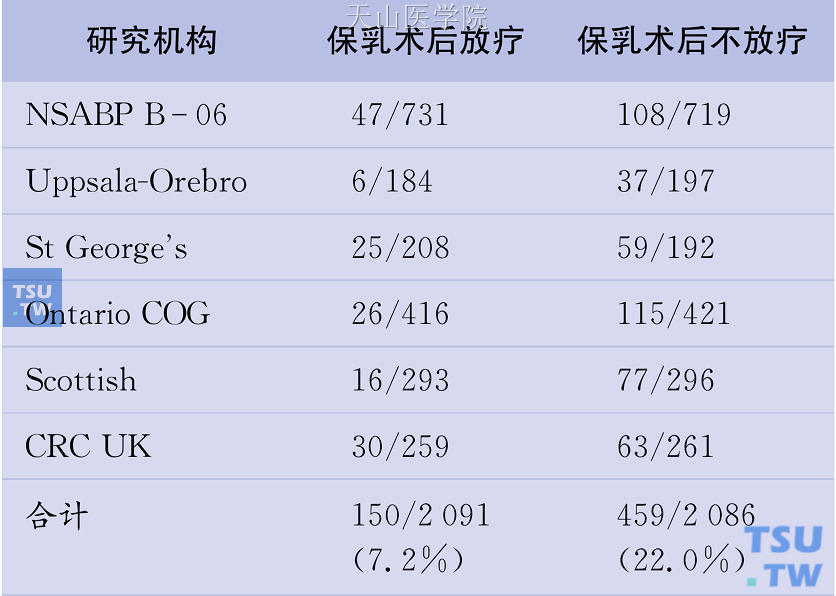
注:NSABP B- 06:国家乳腺和肠道外科辅助治疗计划(美国匹兹堡)。Uppsala-Orebro:乌普萨拉厄勒布鲁癌症研究小组(瑞典乌普萨拉)。St George's:圣乔治医院(英国伦敦)。Ontario COG:安大略临床肿瘤学组(加拿大多伦多)。Scottish:苏格兰癌症试验办公室(英国爱丁堡)。CRC UK:癌症研究项目(英国伦敦)。
保乳术后的美容效果评估
我国一些医院开展的保乳术后美容效果评估是参照欧美国家肿瘤中心提出的标准,另一些医院则自定标准,还有一些医院索性以医患双方的满意度来评估,致使评估结果无法汇总分析和比较。而且保乳术后的美容效果往往是通过参与保乳治疗的医务人员进行,而不是通过除医患双方以外的第三方进行,其客观性存在欠缺,这也是目前我国与欧美国家临床研究存在的不同之处。
1.欧美国家保乳术后评估美容效果的标准
(1)Rose等的方法:以患侧乳房水肿、皮肤凹陷、纤维化、毛细血管扩胀、上臂水肿等作为保乳手术后乳房美容效果评估项目,分为优、良、差3个等级。
(2)放射治疗联合中心(JCRT)标准:优秀(excellent),患侧与健侧乳房相似;好(good),患侧与健侧乳房有细小差别;一般(fair),患侧与健侧相比有较明显差别;差(poor),患侧乳房出现较严重的并发症。
(3)米兰试验组的方法:自保乳治疗后18~24个月起,给患者摄取正面相,然后通过计算机测量两侧乳头水平高度的差值、两侧乳房下皮肤皱褶高度的差值、胸骨中线与两侧乳头水平距离的差值。
(4)根据乳房顺应性的测定进行评估:乳房顺应性即患者站立位与仰卧位时,从乳房的正面观,两侧乳头与乳房下皮肤皱褶距离的差值。在100例正常对照中,上述差值平均数为1.8cm。
(5)其他方法:肿瘤放射协作组(RTOG)/欧洲癌症治疗研究组织(EORTC)SOMA - LENT评分,针对保乳治疗后乳腺组织对称性、皮下脂肪及皮肤水肿、纤维化等项目进行评估,共分4级;Harris评分,通过患侧乳房与健侧乳房的比较进行美容效果评估;采用软件系统进行保乳手术后美容效果评估(BCCT.core软件系统)等。
2.我国保乳术后评估美容效果的标准
(1)我国10家三甲医院共同承担的国家“十五”科技攻关课题——早期乳腺癌规范化保乳综合治疗研究课题组参照国际标准制订了保乳治疗美容效果评估标准。
1)优、良:双乳对称,双侧乳头水平差距≤2cm;患侧乳房外形与健侧无明显差异,外观正常;手感患侧与健侧无差别,皮肤正常。
2)一般:双乳对称,双侧乳头水平差距>2cm,且≤3cm;患侧乳房外形基本正常或略小于健侧;手感患侧略差,皮肤颜色变浅或发亮。
3)差:双乳明显不对称,双侧乳头水平差距>3cm;患侧乳房外观变形,并较健侧明显缩小;手感差,皮肤厚,呈橡皮样,粗糙。
(2)我国卫生部发布的《乳腺癌诊疗规范(2011年版)》推荐的保乳手术后美容效果评价标准
1)很好:患侧乳腺外形与对侧相同。
2)好:患侧乳腺与对侧稍有不同,差异不明显。
3)一般:患侧与对侧有明显不同,但无严重畸形。
4)差:患侧乳腺有严重畸形。
保乳手术技术操作
保乳手术的切口设计
保乳手术的切口设计既要有利于手术解剖,又要获得较理想的乳腺形体效果。按美国NSABP推荐的肿瘤切除与腋窝淋巴结清扫分别做切口。肿瘤位于乳头上方者做弧形切口,肿瘤位于乳头下方者做放射状切口,腋窝解剖另做切口(图27-2、图27-3)。保乳手术原发灶的切缘检测非常重要,术后局部复发与手术切缘不净关系密切,保乳手术要求镜下切缘阴性。2005年意大利米兰保乳共识会议上大多数放射肿瘤学专家认为,浸润性导管癌安全切缘至少1~2mm。
腋窝淋巴结清扫术技术操作
保乳手术是由乳房手术和腋窝淋巴结手术两部分组成。遵循恶性肿瘤的无瘤观念,应首先进行腋窝部位手术,再进行乳房手术,术前已确定腋窝淋巴结转移患者除外。
腋窝淋巴结清扫是保乳手术的组成部分,因切口小、解剖范围广,手术操作应精细;为避免损伤血管、神经,应先显露腋静脉。具体方法:平行于腋褶线,在其下方做弧形切口,长5~6cm。皮肤切开后牵开皮缘,剥离两侧皮瓣,内侧皮瓣剥离至胸大肌外侧缘,外侧皮瓣剥离至背阔肌前缘。沿胸大肌外侧缘向上方解剖,可见到腋静脉前方的喙锁胸筋膜,用镊子将其提起并剪开喙锁胸筋膜后即可显露腋静脉。腋静脉有几支大的血管分支,如胸肩峰血管的胸肌支和胸外侧血管,切断后丝线结扎。沿腋静脉向内侧扩大解剖范围,用拉钩向内侧拉开胸大肌,清扫位于胸大肌、胸小肌之间的Rotter淋巴结。再进一步将胸小肌向内上方拉开,显露和清扫胸小肌后侧组淋巴结,即Ⅱ水平淋巴结。在胸壁前锯肌外侧0.5~1cm处可发现胸长神经,注意加以保护。再沿腋静脉向外侧解剖,显露并保护肩胛下血管及胸背神经。在胸小肌外侧缘至背阔肌前缘之间的淋巴结,包括乳腺外侧组、中央组、肩胛下组及腋静脉淋巴结,即I水平淋巴结(Rotter淋巴结亦归本组)。肋间臂神经即第2肋间神经的外侧皮支,位于腋静脉下方,横穿腋窝淋巴脂肪组织,到达上臂内侧与内侧皮神经会合,应尽量保留该神经。此时腋静脉前方、后方和下方,肩胛下肌前方的所有脂肪结缔组织及I水平、Ⅱ水平的所有淋巴结全部清扫。标本切除后应仔细检查创面,认真止血,并用蒸馏水或生理盐水冲洗手术野。用蒸馏水冲洗的目的是想利用它的低张作用破坏脱落肿瘤细胞的细胞膜,减少肿瘤种植。为避免术后积液,于腋窝部位放置一根多孔引流管,戳口引出连接负压球吸引。此时可以缝合切口,亦可在完成乳腺病灶切除后一并缝合。切口可一层缝合,亦可两层缝合。两层缝合可先用可吸收线行深部真皮间断缝合,使皮瓣靠拢,再用3-0或4-0可吸收线或尼龙线连续皮内缝合,外敷无菌纱布。若不影响下面的病灶切除,亦可通过旋转托手板适当收回外展上肢,增加对腋窝手术区的压力,减少手术创面的渗出。对于临床检查未发现腋窝淋巴结转移的患者,可通过前哨淋巴结活检来了解腋窝淋巴结的状况。
乳腺肿瘤切除术技术操作
按设计好的切口切开皮肤,为扩大切除范围需潜行剥离皮瓣,剥离范围由切除范围决定。若肿瘤边界清楚,至少切除肿瘤周围1cm的正常组织;若肿瘤边界不甚清楚,应适当扩大切除范围。由皮下、腺体直至胸肌筋膜,连同肿瘤表面的皮肤一并切除。若肿瘤边缘不整齐,可疑部位切缘应进行术中冷冻切片病理检查。若切缘镜下阳性,还应补切;若多次冷冻切片病理检查阳性,应放弃保乳手术。肿瘤标本离体后应即刻对其上方及内侧进行标记,相对应的即为下方及外侧,基底若能明显辨认则不必标记。目的是方便术后病理科医师了解标本的方位,并对四周切缘及基底进行病理学检查(图27-5)。如肿瘤切除范围小,可直接缝合皮肤(皮内缝合),不放引流,残腔由血清和纤维蛋白渗出充填,保持原病灶区轮廓。如肿瘤切除范围较大,彻底止血后应将残腔四周的腺体拉拢缝合;若缝合以后原瘤床部位不能位于缝合切口的正下方,则应在腺体拉拢缝合前在残腔四周留置标记再拉拢缝合,有利于术后放疗科医师确定推量照射的靶区范围。如手术医师术中采取留置标记的方法定位瘤床,术前应告知患者及家属,并签署知情同意书。皮肤切口可行一层(皮内缝合)或两层缝合。连同腋窝部切口,可用胸带包扎固定。
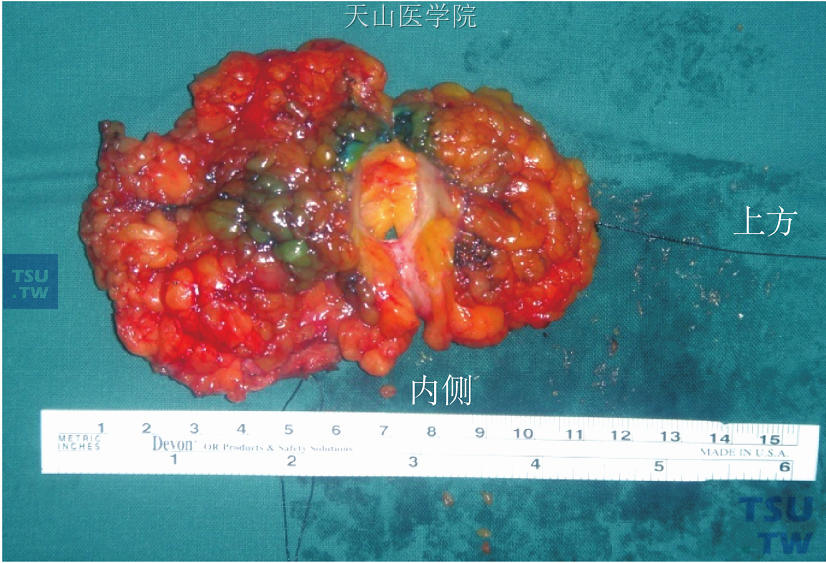
图27-5 保乳手术乳房肿瘤切除标本,以手术线标记方位,1根丝线为上方,2根丝线为内侧,以便病理检测切缘时能明确标本方位
