基因的突变和调控失常往往与肿瘤的发生发展有关。目前,许多乳腺癌相关基因,包括多种癌基因、抑癌基因、遗传易感性基因都被证明与乳腺癌的生物学性质密切相关,其表达或突变具有对化疗、内分泌治疗、靶向治疗的预测价值,并影响患者的预后。常用乳腺癌相关基因见表22-7。
表22-7 乳腺癌相关基因

HER-2/neu
HER-2/neu是表皮生长因子受体家族成员之一,定位于染色体17q21。HER-2蛋白在正常的乳腺细胞中低表达,而在20%~30%的乳腺癌中可过度表达。在乳腺癌中,原位癌与转移性乳腺癌中的HER-2表达可能要高一些。HER-2是乳腺癌重要的预测和预后因子,其应用于临床的论证见表22-8。
表22-8 HER-2应用于临床的论证
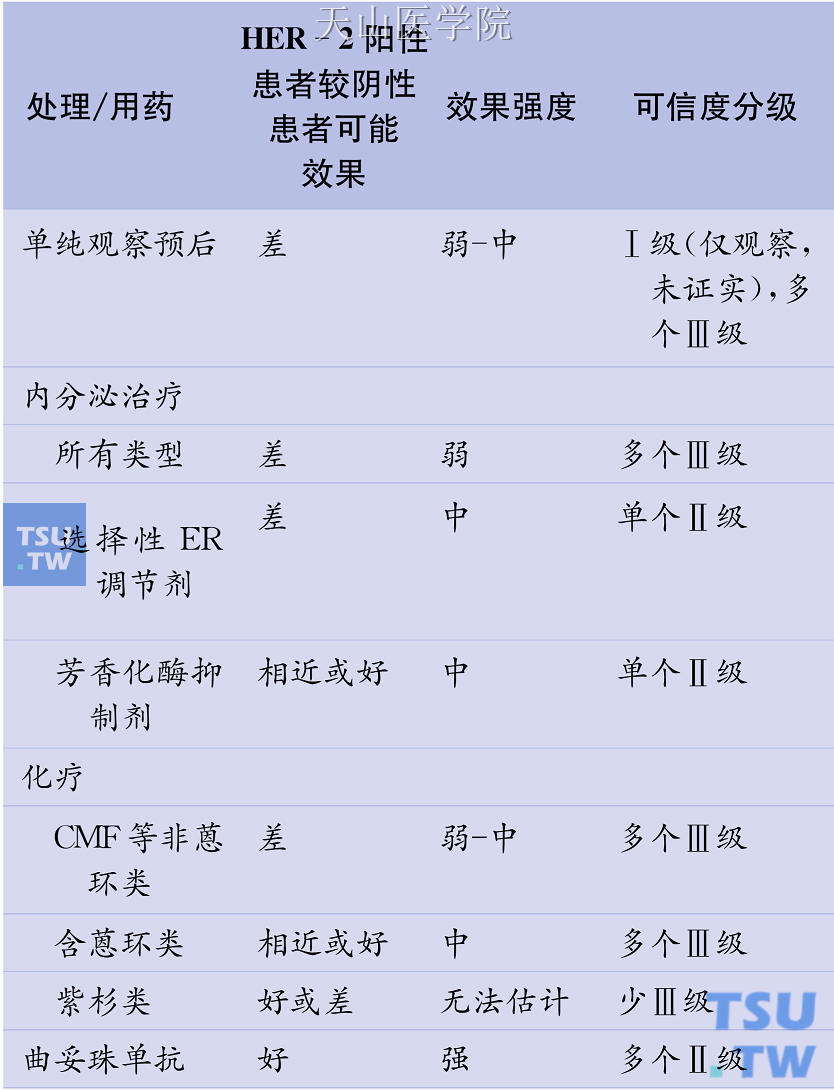
HER-2过表达(免疫组化3+或FISH阳性)对于针对HER-2的靶向治疗(如曲妥珠单抗)具有重要的预测价值。此外,HER-2表达是第一个用于预测化疗疗效的因子。HER-2阳性乳腺癌对于含蒽环类的化疗方案,相比CMF化疗方案更为敏感。对于紫杉类方案,有报道指出HER-2过表达患者对含有多西他赛的化疗方案效果较好。NSABP-11研究也证实,对于HER-2阳性患者,含多西他赛的化疗能够提高DFS和OS。目前针对HER-2在内分泌治疗疗效预测中的作用存在着一定的争议,个别研究指出,HER-2基因扩增或蛋白过表达患者易对他莫昔芬耐药。
在多数研究中,未经治疗的原发肿瘤中HER-2过表达(免疫组化检测)与较差的预后相关。HER-2过表达肿瘤通常具有较高的细胞核分级、较大的体积、较多的淋巴结转移。一般公认在淋巴结阳性患者中,HER-2过表达是预后不良的标志。而在淋巴结阴性患者中,其预后意义仍存在一定的争议。在一项包含2 026例淋巴结阴性乳腺癌患者的回顾性研究中,70%的患者并未接受辅助性治疗,HER-2过表达与相对较差的10年RFS率相关(66%与76%)。在这项研究中,大约90%的肿瘤超过1cm。此项研究为曲妥珠单抗在淋巴结阴性、肿瘤大小>1cm患者中的应用提供了可靠的依据。因此,HER-2过表达被广泛认可为早期乳腺癌患者有必要接受化疗的依据之一。尽管如此,由于患者预后往往被后续靶向治疗所影响,在实际临床工作中HER-2的预后指标意义仍有待商榷。
此外,在血清学方面,大约30%的转移性乳腺癌患者存在血清HER-2胞外域(ECD)水平的升高,并且这一高水平表达与较差的预后相关。在早期乳腺癌中,升高的HER-2 ECD水平同样标志着更高的复发转移风险。但由于ECD水平直接取决于肿瘤负荷量的大小,并且缺乏足够的证据表明其预后价值,血清HER-2 ECD水平并不作为临床实践中的推荐检测项目。
EGFR
EGFR基因又称HER-1基因,定位于染色体7pll~13,产生5.8~10kb的mRNA,其蛋白质产物为表皮生长因子受体(EGFR),是一种具有酪氨酸蛋白激酶活性的细胞受体,其与相应的配体EGF、TGF结合后,通过细胞内信号转导,引起细胞过度分裂、增殖及恶变。
EGFR的检测方法有RNA印迹法(Northern blotting)或免疫组化法。几乎所有的报道都认为EGFR与激素受体状态负相关。激素受体阴性者,EGFR阳性,EGFR的表达与肿瘤细胞的分化密切相关。虽然对于EGFR的预后价值还存在一定的争议,但多数单因素分析表明,EGFR高表达组的预后明显差于低表达组。随着随访时间的延长,这种趋势逐渐缩小。Harris等证实EGFR对淋巴结阴性病例预测预后的价值较淋巴结有转移者为大。
此外,许多研究发现EGFR低表达患者对内分泌治疗效果较好。Nicholson报道ER阳性、EGFR阴性患者,有80%对内分泌治疗有效。同时EGFR也被用来作为生物治疗的靶分子。因此,EGFR也是一个较有前景的预测指标。
p53
p53基因是目前乳腺癌中研究最为透彻的抑癌基因,它位于17号染色体长臂。野生型p53基因能抑制细胞的恶性转化,控制细胞的增长,是细胞生长的负调节因子,突变型P53蛋白质则能促进细胞的恶性转化。具有P53免疫原性的乳腺癌约占50%左右。P53过表达与乳腺癌较差的肿瘤分化及ER有关,与淋巴结转移关系不大,但淋巴结阳性同时P53阳性患者预后相对较差。有关P53的预后价值,目前的观点存在着争议。有些研究者认为有突变型P53的淋巴结阴性患者其生存期较短,然而另一些作者却否认它们存在相互关系。也有报道提出P53的检出与对化疗较好的反应性有关。
bcl-2
bcl-2基因是凋亡研究中最受重视的癌基因之一,它首先从滤泡型B细胞淋巴瘤的14和18染色体t(14:18)易位断裂点克隆,其染色体异位导致蛋白产物的过表达。虽然对凋亡的调节机制目前还不完全清楚,但Bcl-2是体内外抑制细胞凋亡的重要因子已被证实,其基因产物广泛分布于许多正常组织,也可见于乳腺癌、消化道肿瘤等。bcl-2表达能够抑制肿瘤细胞的凋亡,因此某些学者提出其高表达与较差的预后相关。同时,也有研究者提出,Bcl-2蛋白是由雌激素调节的,此蛋白多局限在那些内分泌受体阳性乳腺癌细胞中,从而高表达Bcl-2蛋白的乳腺癌患者能够在内分泌治疗中获益。近年来,随着细胞自噬研究的不断发展,有研究者提出作为细胞自噬重要调控蛋白Beclin-1的抑制基因——bcl-2能够通过抑制细胞自噬影响肿瘤对化疗、放疗的耐受性。这些结论仍有待于进一步研究的证实。
nm23
nm23基因定位于染色体17q21.3,由5个外显子、24个内含子组成。转录片段为0.8kb,使用限制性片段长度多态性(RFLP)及单链构象多态性(SSCP)方法发现该基因在多种实体瘤中的变化主要表现为等位基因的丢失。人类nm23基因分为nm23-H1及nm23-H2两种类型。
乳腺癌是nm23基因研究较多的肿瘤之一。Hennessy等对71例乳腺癌研究发现nm23基因转录水平与肿瘤分化程度、腋窝淋巴结转移直接相关,而与肿瘤大小、激素受体水平、EGFR等无关。Barnes等用免疫组化研究发现nm23高表达者存活期长,提示nm23是一个独立的预后指标。Heimann对163例淋巴结阴性的患者进行多因素分析发现,nm23高表达组的相对复发危险系数为0.38。
p16
p16(CDK N2/MTS1)基因最早在黑色素瘤患者中发现,位于人9号染色体,全长8.5kb,由2个内含子和3个外显子构成。该基因编码一种由307个氨基酸组成的相对分子质量为16 000的蛋白,可通过抑制细胞分裂周期的关键酶CDK4,抑制细胞生长,在细胞周期中起负性调节的作用。p16基因发生结构突变和功能缺失,则细胞旺盛分裂,最终失去控制。60%的乳腺癌细胞系存在p16基因纯合子缺失,可作为检测肿瘤的预后指标。
BRCA-1
BRCA-1基因是目前所发现的最重要的乳腺癌易感基因之一,其突变形式主要为终止码突变、错义突变和移码突变,在遗传性乳腺癌家系中突变率约45%。BRCA-1是调控细胞周期G/M期关键点的调控因子,是激活Chkl激酶所必需的,而后者对DNA损伤时诱导G/M期阻滞起重要作用。同时,BRCA-1还可控制Cdc25C和Cdc2/细胞周期蛋白B1激酶蛋白的表达、磷酸化以及胞内定位的调节,这两种蛋白对细胞周期G/M期的顺利进行起重要作用。BRCA-1表达与雌激素及其受体有着密切关系,与乳腺癌组织学分级、淋巴结转移程度呈正相关,与患者年龄、ER、PR呈负相关。
